目次
CBL(Casitas B-lineage Lymphoma)遺伝子は、第11番染色体長腕(11q23.3)に位置し、RINGフィンガー型E3ユビキチンリガーゼをコードする、後生動物に広く保存された重要な遺伝子です。細胞内では本来、受容体チロシンキナーゼ(RTK)の過剰シグナルを遮断する「腫瘍抑制因子」として働きますが、特定の領域に変異が生じると一転して強力な「がん遺伝子」へと変貌するという稀有な「二面性(Dual Personality)」を持ちます。この生化学的パラドックスが、JMML・CMML・AMLなどの骨髄系腫瘍から固形腫瘍、さらには全身性の発達症候群(CBL症候群)まで、多彩な疾患の分子基盤となっています。
Q. CBL遺伝子とはどのような遺伝子ですか?まず結論だけ知りたいです
A. 第11番染色体(11q23.3)に位置するRINGフィンガー型E3ユビキチンリガーゼをコードする遺伝子です。正常ではRTKシグナルを負に制御する腫瘍抑制因子として機能しますが、LHRまたはRINGドメインに変異が生じるとE3リガーゼ活性を失いつつアダプター機能を維持し、がん遺伝子へと変貌するという「二面性」が最大の特徴です。JMML(約15%)・CMML(10〜15%)・AML等の骨髄系腫瘍のほか、生殖細胞系列変異によるCBL症候群の原因遺伝子でもあります。
- ➤遺伝子の基本情報 → 11q23.3、3つのホモログ(c-CBL・CBL-b・CBL-c)、E3ユビキチンリガーゼの役割
- ➤分子メカニズム → 自己抑制構造・Y371リン酸化による活性化・変異によるE3活性喪失とアダプター暴走
- ➤骨髄系腫瘍 → JMML(LHR変異・生殖細胞系列85%)・CMML(RINGドメイン変異)・AML(セカンドヒット)の比較
- ➤CBL症候群 → ヌーナン様症候群・JMMLの自然退縮・Watch and Wait戦略の最新エビデンス
- ➤最新治療 → FLT3阻害薬・CBL-b阻害剤NX-1607の臨床試験・免疫腫瘍学アプローチ
1. CBL遺伝子とは:発見の経緯と生物学的位置づけ
CBL遺伝子は、もともとマウスの白血病や線維芽細胞のトランスフォーメーションを引き起こすレトロウイルス(Cas NS-1)の腫瘍遺伝子「v-Cbl」の、細胞内ホモログ(相同遺伝子)として最初に同定されました。哺乳類においては、c-CBL(一般にCBLと呼ばれる)・CBL-b・CBL-cの3つのホモログが存在し、それぞれが細胞増殖、分化、そして免疫応答の制御において重要な役割を担っています。
💡 用語解説:E3ユビキチンリガーゼとは
細胞内でタンパク質に「分解の目印」を付ける酵素の一種です。この目印となる小さなタンパク質が「ユビキチン」で、ユビキチンが付いたタンパク質はプロテアソーム(細胞内のゴミ処理装置)やリソソームで分解されます。E1・E2・E3という3種類の酵素が順番に働きますが、E3リガーゼが「どのタンパク質を分解するか」を決める最重要の鍵です。CBLファミリーはRINGフィンガー型E3リガーゼとして、主に受容体チロシンキナーゼを標的としています。
💡 用語解説:受容体チロシンキナーゼ(RTK)とは
細胞膜に存在し、成長因子などの外部刺激を受け取ると細胞内にシグナルを伝える受容体タンパク質の一群です。EGFR・FLT3・KDRなどが代表例。RTKが過剰に活性化すると際限のない細胞増殖・生存シグナルが発せられ、がん化の主要な原因となります。CBLはこのRTKをユビキチン化して分解する「緊急停止ボタン」の役割を果たしています。
腫瘍抑制因子とがん遺伝子の「二面性」——CBLの核心
CBLタンパク質の本来の働きは、活性化されたRTKや非受容体型チロシンキナーゼに結合してユビキチン化し、プロテアソームまたはリソソームでの分解へと導くことで過剰な増殖シグナルを遮断する「腫瘍抑制因子」です。しかし、CBL遺伝子に変異が生じると状況は一変します。E3ユビキチンリガーゼ活性が失われると同時に、シグナル伝達分子を動員する「アダプタータンパク質」としての機能が維持・強化され、結果として発がんを促進する「がん遺伝子」として振る舞うようになります。この「二面性(Dual Personality)」こそが、CBLの生物学的機能と発がんメカニズムを理解する上での核心です。
3つのホモログの中でも、c-CBL(本記事で主に扱うCBL)は骨髄系細胞に高く発現しており、造血器腫瘍との関連が最も深く研究されています。一方、CBL-bは主にTリンパ球・Bリンパ球・NK細胞に高発現し、免疫応答の抑制制御を担う重要な分子です(詳細はSection 7「治療戦略」にて解説)。
2. タンパク質構造と分子制御メカニズム
CBLタンパク質は複数の機能ドメインからなる高度に組織化された足場(スキャフォールド)タンパク質であり、その構造的完全性がシグナル伝達の精密な制御に不可欠です。以下の各ドメインの連携によって、CBLの活性は厳密に制御されています。
自己抑制構造とリン酸化による活性化
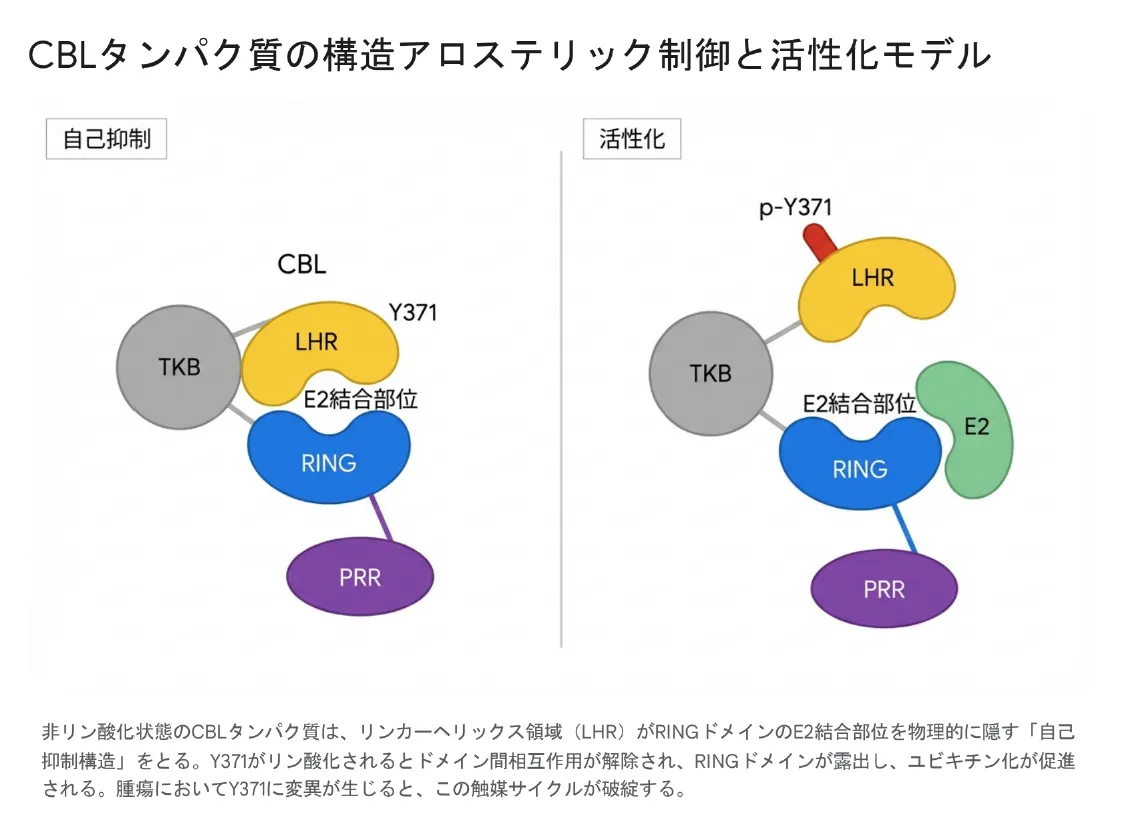
CBLタンパク質は細胞内で常に活性状態にあるわけではなく、非常に厳密なアロステリック制御下に置かれています。NMR(核磁気共鳴)やSAXS(小角X線散乱)を用いた構造生物学的解析から、非リン酸化状態のCBLは「自己抑制型(autoinhibited conformation)」と呼ばれるコンパクトで閉じた立体構造をとることが明らかになっています。この状態では、N末端のTKBドメインとLHRが分子内で強固に相互作用し、RINGドメイン上のE2酵素結合表面を物理的に覆い隠しています。
💡 用語解説:アロステリック制御とは
タンパク質のある部位(アロステリック部位)への分子の結合が、離れた別の部位(活性部位)の構造や機能を変化させる制御機構です。CBLでは、LHRのY371がリン酸化されると、離れた位置にあるRINGドメインのE2結合面が露出されるという「離れた場所への連鎖的な構造変化」がアロステリック制御の典型例です。まるでドアノブを回すと別の場所の錠前が開くような仕組みです。
細胞外からの成長因子刺激によってシグナル伝達経路が活性化されると、TKBドメインを介してCBLが標的キナーゼに動員されます。続いて、標的キナーゼまたはSrcファミリーキナーゼがLHRの重要なチロシン残基(CBLではY371)をリン酸化します。このリン酸化によって導入された負電荷がドメイン間の静電的反発を引き起こし、CBLの立体構造に劇的な変化をもたらします。結果として、TKBドメインによるRINGドメインのマスキングが解除され、E2結合表面が露出するとともにEGFRなどの受容体の効率的なユビキチン化と分解が実行されます。
非リン酸化状態(自己抑制)ではLHRがRINGドメインのE2結合部位を隠しているが、Y371がリン酸化されると(活性化)ドメイン間相互作用が解除され、RINGドメインが露出してユビキチン化が促進される。腫瘍においてY371に変異が生じると、この精密な制御サイクルが破綻する。
💡 用語解説:SLAP/SLAP2による代替活性化経路
標準的なキナーゼ依存性の活性化に加え、SLAP(Src-like adaptor protein)およびSLAP2というアダプタータンパク質がCBLの活性を制御する代替経路も存在します。SLAP2のC末端αヘリックスがCBLのTKBドメインに結合することで自己抑制構造を物理的に解除し、抗原受容体やサイトカイン受容体のシグナルダウンレギュレーションにおいて重要な役割を果たしています。キナーゼ非依存的な活性化経路として免疫応答の精密な調節に貢献しています。
3. 変異によるがん化メカニズム——二面性のパラドックス
CBLが細胞レベルではRTKのシグナルを遮断する腫瘍抑制因子であるにもかかわらず、歴史的に白血病を惹起する「がん遺伝子」として最初に同定された背景には、分子生物学的なパラドックスが存在していました。この矛盾は、腫瘍細胞で生じるCBLの構造的変異がもたらす「腫瘍抑制機能の喪失」と「がん遺伝子機能の維持・強化」という二重のメカニズムによって見事に説明されます。
E3リガーゼ活性の喪失とアダプター機能の暴走
骨髄系腫瘍などの臨床検体から同定された変異型CBLの解析により、疾患関連ミスセンス変異の大部分がLHR(特にY371周辺)またはRINGドメイン周辺に高度に集中していることが明らかになっています。Y371E・Y371S・Y371D・Y371C・Y371Hといった特定の変異はタンパク質の動態を根本的に変化させ、CBLを溶液中で物理的に「伸びた(extended)」構造に変化させてRINGドメインを持続的に露出させます。しかしながら、同時にE2酵素の動員とユビキチン転移に不可欠なキナーゼによるリン酸化反応が不可能となり、E3リガーゼ活性は完全に喪失します。
一方で、これらのミスセンス変異はN末端のTKBドメインやC末端のPRRおよびチロシンリン酸化部位を無傷のまま残します。その結果、変異型CBLは活性化されたRTKに結合する能力を維持し、巨大なスキャフォールドとして機能し続けます。本来であれば速やかに分解されるべき受容体が細胞膜上に蓄積する環境下で、変異型CBLはPI3K/AKT経路やSTAT5経路などの生存・増殖シグナルを持続的かつ異常に活性化させる「がん遺伝子」として機能します。
💡 用語解説:アダプタータンパク質とは
それ自体は酵素活性を持たず、複数の分子を物理的に近づけることでシグナルを伝える「中継役」のタンパク質です。CBLは正常ではE3リガーゼとしてRTKを分解しますが、変異によってE3活性を失ってもアダプターとしてRTKやシグナル分子を繋ぎ続け、増殖シグナルを増幅させるアクセル役に変貌します。「ブレーキが壊れてアクセルになる」という比喩が最もわかりやすい変化です。
LYNキナーゼによるPI3K/AKT経路の増幅ループ
CBL変異細胞のプロテオミクス解析により、LYNキナーゼの活性化と変異型CBLへの結合が顕著に亢進していることが示されています。LYNはCBLのC末端にあるY731を強力にリン酸化し、これによりPI3KのサブユニットであるPIK3R1(p85)のリクルートがさらに増強されて下流のAKTシグナルが劇的に増幅するという正のフィードバックループが形成されます。ダサチニブによるLYNの薬理学的阻害が、この相互作用を遮断してAKT活性化を抑制できることから、変異型CBLの腫瘍形成においてLYN-PI3K枢軸が決定的な役割を担っています。
片親性ダイソミー(UPD)によるホモ接合化——がん化完成の必須条件
CBL変異による発がんは、単一のヘテロ接合型変異だけでは細胞のトランスフォーメーションを完全に駆動できないことが多いとされています。野生型(正常な)CBLアレルが残存していると、野生型タンパク質が変異型と競合してRTKに結合し、正常にユビキチン化してシグナルを遮断してしまうからです。この分子レベルの競合を克服するため、CBL変異を持つ腫瘍細胞は進化の過程で第11番染色体長腕(11q)における「片親性ダイソミー(UPD)」を極めて高い頻度で引き起こします。
💡 用語解説:片親性ダイソミー(UPD)とは
通常、私たちの染色体は父親由来と母親由来の2本を1セットとして持ちます。片親性ダイソミーとは、片方の親からの染色体が2本(ホモ接合体)になり、もう一方の親の染色体が消失する状態です。11q UPDが生じると、変異型CBLアレルが複製されてホモ接合体となり、野生型CBLアレルが物理的に喪失(ヘテロ接合性の喪失:LOH)します。骨髄系腫瘍で同定されるCBLミスセンス変異の約83%はホモ接合型として検出され、ほぼ例外なく11q UPDに起因しています。
エクソン8/9欠失変異によるFLT3シグナルの恒常的活性化
ミスセンス変異に加えて、スプライス部位の異常やインデルによって引き起こされるCBL遺伝子のエクソン8またはエクソン9のインフレーム欠失バリアントが、AMLやMDSの特定のサブセットで同定されています。エクソン8/9の欠失はLHRの遠位部からRINGフィンガードメインの近位部を丸ごと喪失させることを意味し、E3リガーゼ活性を完全に破壊します。この変異体(CBL-70Zなど)の特筆すべき点は、造血器腫瘍において極めて重要な受容体であるFLT3と相互作用し、FLT3の細胞内インターナリゼーションを阻害することでFLT3経路を恒常的に自己活性化させる能力を持つことです。これは最新の分子標的治療(FLT3阻害薬)の治療標的として直接結びついています。
4. 骨髄系腫瘍におけるCBL変異の病態と臨床的特徴
CBL変異は特定の造血器腫瘍、とりわけ骨髄系腫瘍において高い頻度で認められ、その病態形成の主要なドライバーとして機能しています。代表的な疾患であるJMMLとCMMLを中心に、その臨床像と分子的背景を分析します。
若年性骨髄単球性白血病(JMML)における役割
💡 用語解説:JMML(若年性骨髄単球性白血病)とは
主に乳幼児期(中央値2歳)に発症する極めて稀で予後不良な血液がんで、骨髄増殖性と骨髄異形成性の両方の特徴を持つ交雑腫瘍です。臨床的には貧血・白血球増多・単球増多・血小板減少・肝脾腫を特徴とします。患者の約95%がRAS/MAPK経路(PTPN11・KRAS・NRAS・NF1・RRAS・RRAS2・SH2B3・CBL)のいずれかに変異を有しており、このうちCBL変異をドライバーとする患者は全体の約15%を占めます。
JMMLにおけるCBL変異の最も重要な特徴は、変異の約85%が後天的な体細胞変異ではなく「生殖細胞系列変異(Germline mutation)」——つまり全身の細胞に先天的に存在する変異——であることです。成人領域の白血病とは著しく異なるこの特徴が、CBL症候群(後述)との関連を生み出しています。発症には、造血幹細胞においてのみ二次的なイベント(11q UPDによるLOH)が生じてホモ接合化することが引き金となります。
重要:JMMLと診断された全例において、末梢血の所見やDNAメチル化プロファイリングだけでは体細胞変異例と生殖細胞系列変異例を正確に区別できないため、JMMLと診断された全患者に生殖細胞系列の遺伝子検査(Germline testing)を実施することが強く推奨されています。また体細胞変異のみの約15%の患者群は、生殖細胞系列変異群と比較して、より攻撃的な臨床経過をたどる傾向があります。
慢性骨髄単球性白血病(CMML)および急性骨髄性白血病(AML)への関与
💡 用語解説:CMML(慢性骨髄単球性白血病)とは
成人に発症する稀な造血器腫瘍で、GM-CSF(顆粒球マクロファージコロニー刺激因子)に対する過敏性など、JMMLと多くの生物学的特徴を共有しています。患者全体の約10〜15%においてCBL変異が同定されますが、JMMLとは異なりRINGフィンガードメインに変異が集中する傾向(P<0.0001)があり、分子的背景に明確な差異があります。TET2(75%)・ASXL1(58%)・SRSF2(50%)などのエピジェネティック制御・スプライシング関連遺伝子との共存変異が高頻度に認められます。
CMMLにおけるCBL変異患者は、野生型患者と比較して、診断時の骨髄芽球割合の増加・著明な白血球増多・重度の脾腫などのより強い「増殖性」表現型(MP-CMML)を示します。この強い増殖能の根底には、CMMLのCD34陽性幹細胞および前駆細胞においてCD116(GM-CSF受容体α鎖)およびCD131の共発現と受容体密度が著しく上昇していることがあり、GM-CSFに対する異常な過敏性と細胞増殖を裏付けています。また一人の患者骨髄内に複数の異なるCBL変異サブクローンが混在する複雑なクローン構造を持つケースが64%に上ることも報告されています。
AMLにおいては、MDSや他の骨髄増殖性疾患から進展した二次性AMLの約10%、および非定型慢性骨髄性白血病(aCML)の約8%でCBL変異が認められます。家族性血小板異常症/AML(FPD/AML)に関連するRUNX1変異を持つ患者において、CBL変異と11q-aUPDの獲得がMDSまたはAMLへの白血病化を引き起こす重要な「セカンドヒット」として機能しているという知見も、疾患進行を予測するバイオマーカーとして注目されています。
JMML対CMML:CBL変異陽性骨髄系腫瘍の特徴比較
JMMLではLHR変異が支配的であり生殖細胞系列の関与が多いのに対し、CMMLではRINGドメイン変異が多く、TET2などのエピジェネティック二次変異との高い共存率を示す。
5. CBL症候群:生殖細胞系列変異が引き起こす多臓器症候群
CBL遺伝子の生殖細胞系列変異は、全身性の発達異常・形態異常・特定のがんへの顕著な感受性を伴う稀な多発奇形症候群を引き起こします。この疾患単位は臨床遺伝学において「CBL症候群」あるいは「JMMLを伴うヌーナン様症候群(Noonan syndrome-like disorder with JMML)」として分類されています。
💡 用語解説:ヌーナン症候群との類似性
ヌーナン症候群は低身長・先天性心疾患・特徴的顔貌などを呈する比較的よく知られた先天異常症候群です。CBL症候群は顔の形や心疾患などヌーナン症候群と酷似した表現型を持つため「ヌーナン様症候群」と呼ばれますが、原因遺伝子はCBLであり、特にJMMLを発症する確率が高いという点で独立した疾患単位として分類されています。同じ家族内でも症状の重さは大きく異なります。
多臓器にわたる臨床的特徴
CBL症候群は常染色体顕性遺伝(Autosomal dominant)の形式をとり、変異遺伝子を1つ受け継ぐだけで発症し得ます。ただしその表現型や浸透率は同一家系内でも大きなバリエーションを示し、症状が非常に軽微で成人まで見過ごされるケースがある一方、乳児期から重篤な発達障害を呈するケースも存在します。
👤 頭蓋顔面・発育
- 広い額・前頭部の突出
- 眼窩開離(hypertelorism)
- 眼瞼下垂(ptosis)・斜視
- 低位耳介・後方回転した耳
- 厚い口唇・深く長い人中
- 一部で小頭症(microcephaly)
🦴 成長・筋骨格系
- 出生後の成長遅延・低身長
- 翼状頸(pterygium colli)
- 外反肘(cubitus valgus)
- 著明な筋緊張低下(hypotonia)
- 手指を中心とした関節過可動性
❤️ 心血管・外胚葉
- 大動脈弁狭窄症・二尖弁
- 心筋症のリスク
- 停留精巣(cryptorchidism)
- 薄く疎な頭髪
- カフェオレ斑
⚠️ 稀な重篤合併症
- 羊水過多(胎児期)
- リンパ漏(乳び胸)
- 血球貪食性リンパ組織球症(HLH)
- 血管炎・もやもや病
💡 用語解説:もやもや病(Moyamoya disease)とは
脳の主要な血管(内頸動脈)が徐々に閉塞し、代償として細い側副血管(もやもや血管)が増生する進行性の脳血管疾患です。脳梗塞や脳出血のリスクが高まります。CBL変異を有するJMML患者では自己免疫性の機序が疑われる血管炎ともやもや病の合併が複数報告されており、MRA(磁気共鳴血管画像)を用いた血管炎合併のプロスペクティブなスクリーニングが強く推奨されています。
JMMLの「自然退縮」という驚くべき生物学的特異性
CBL症候群における最も重大な臨床的課題は、乳児期に極めて高い確率でJMMLを発症することです。しかし、生殖細胞系列のCBL変異に起因するJMMLは、他のがん遺伝子(PTPN11やNF1など)に起因する典型的なJMMLとは全く異なる、驚くべき生物学的振る舞いを見せます。
一般的なJMMLが急速に進行し、同種造血幹細胞移植(HSCT)なしには致死的となるのに対し、生殖細胞系列CBL変異によるJMMLの大部分は、強力な化学療法や骨髄移植を行わなくても、時間の経過とともに「自然退縮(Spontaneous resolution)」を遂げるという特異な現象が多数確認されています。驚くべきことに、これらの患者の骨髄細胞においては11q UPDによる変異クローンによる造血が継続しているにもかかわらず、白血球増多や脾腫といった異常な骨髄増殖性の臨床症状が次第に沈静化し、血液学的な正常化に至ります。
💡 自然退縮のメカニズム(現在提唱されている仮説)
- 過剰なRAS/MAPK経路活性化に対する細胞内のネガティブフィードバック機構が順応する
- GM-CSFなどの増殖サイトカインへの感受性が加齢に伴って生理的に減弱する
- CBL変異型JMMLが持つ低メチル化(Low-methylation profile)エピジェネティックプロファイルがTET2などの二次体細胞変異の蓄積を抑制し、疾患の悪性化を免れさせている
「Watch and Wait」アプローチへのパラダイムシフト
この特異な生物学的挙動に基づき、近年の国際的な小児血液腫瘍の管理ガイドラインではパラダイムシフトが起きています。フランスの161例に及ぶ大規模コホート研究(Neven et al., Blood 2026)などのリアルワールドデータにより、全体の約3分の1のJMML患者(特にCBL変異や一部のNRAS変異を持つ低リスク群)は移植を安全に回避できることが実証されました。
💡 用語解説:Watch and Wait(経過観察)アプローチ
直ちに積極的な治療(骨髄移植)を行うのではなく、低用量化学療法(アザシチジン・6-メルカプトプリンなど)を併用しながら厳密な臨床モニタリング下で経過を観察する治療戦略です。生殖細胞系列CBL変異を有するJMML患者においては、現在この戦略が標準的な第一選択として推奨されています。ただし、第7染色体モノソミーなどの染色体異常の追加、明らかな疾患進行(Blast crisis)、重篤な血小板減少による輸血依存状態が見られた場合には、速やかにHSCTの適応となるため、慎重なモニタリングが不可欠です。
6. 固形腫瘍・CNS腫瘍への展開——RTK活性化の普遍的マーカーとして
歴史的に、CBL変異の腫瘍学的意義はJMMLやCMMLといった骨髄系白血病の文脈でのみ広く研究されてきました。しかし、2024〜2025年にかけての最新のゲノム医学の進展により、この認識は大きく覆されつつあります。
「ZERO Childhood Cancer Program」などの包括的な個別化医療プログラムが実施した全ゲノムシーケンシング(WGS)とRNAシーケンシング(RNAseq)の統合解析により、小児の中枢神経系(CNS)腫瘍および多様な固形腫瘍においても、CBL変異が発がんのドライバーとして極めて重要な役割を果たしていることが新たに証明されました。
小児高悪性度グリオーマ(pHGG)・神経芽腫(Neuroblastoma)・胚細胞腫瘍などにおいて、CBLのリンカー領域やRINGドメインに機能的影響を及ぼす新規のミスセンス変異(CBL E366_E373delやC384Gなど)やスプライシング変異が次々と同定されています。特筆すべき事例として、血液がんでそのトランスフォーメーション能力が知られていた「CBLエクソン8/9欠失変異」が、血液がんとは起源の全く異なる神経芽腫患者の腫瘍において発見されています。機能解析の結果、この変異体はリン酸化EGFRに対するユビキチン化と分解を阻害し、EGFRシグナルを細胞内で恒常的に維持することによって細胞増殖を強力に促進することが実証されました。
🔑 固形腫瘍でのCBL変異が持つ臨床的インパクト
これまで既存のゲノム検査において特定のRTK変異や増幅(EGFR変異・ALK融合遺伝子など)が見つからず、分子標的治療の対象から外れていた難治性の小児がん患者であっても、下流のブレーキ役であるCBLに変異があればRTK経路が異常活性化しているため、既存のチロシンキナーゼ阻害薬(TKI)が著効する可能性があります。CBL変異のプロファイリングは、固形腫瘍におけるプレシジョン・メディシン(精密医療)の適用範囲を大きく拡大するポテンシャルを秘めています。
7. 次世代分子標的治療と免疫腫瘍学アプローチ
CBLは、その機能の二面性と変異による影響が組織・細胞種によって異なることから、治療標的としての戦略は極めて高度かつ文脈依存的です。現在、大きく分けて3つの革新的なアプローチが並行して進められています。
① 異常な下流シグナル伝達経路の直接的阻害
FLT3阻害薬の適用:骨髄系腫瘍におけるCBLエクソン8/9欠失変異などがFLT3受容体を過剰活性化するという明確なメカニズムに基づき、ミドスタウリン・ギルテリチニブ・キザルチニブなどのFLT3阻害薬の適用拡大が検討されています。現在進行中の第I相臨床試験において、キザルチニブとアザシチジンの併用療法がCBL変異を有するMDS/MPN患者のコホートにおいて60%の全奏効率(ORR)という有望な初期応答を示しています。
LYN・PI3K経路の阻害:変異型CBLによる発がんシグナル増幅においてLYNキナーゼが必須の役割を果たすことから、ダサチニブ(マルチキナーゼ阻害薬)によってLYNと変異型CBLの相互作用を遮断することで、CMML細胞の増殖がin vitroおよび患者検体モデルで顕著に抑制されることが実証されており、LYN-PI3K枢軸を標的とした新たな治療オプションとして有望視されています。
② CD116を標的とした細胞表面免疫療法
CMMLにおけるCBL変異細胞は、正常な造血幹細胞と比較してCD116(GM-CSF受容体α鎖)およびCD131の細胞表面での発現量が有意に高く、受容体密度が上昇するという特有の分子的特徴を有します。この事実は、細胞内にある変異型CBLタンパク質を直接標的とするのではなく、細胞表面に過剰発現しているCD116を標的とすることで、CBL変異クローンを選択的に排除できる可能性を示しています。現在、CD116を特異的に認識するモノクローナル抗体・抗体薬物複合体(ADC)・CAR-T細胞療法を用いたアプローチが前臨床段階で開発されています。
💡 用語解説:CAR-T細胞療法とは
患者自身のTリンパ球(免疫細胞)を体外に取り出し、がん細胞の表面抗原を特異的に認識できるように遺伝子操作(Chimeric Antigen Receptor:キメラ抗原受容体を搭載)してから体内に戻す先進的な細胞療法です。CD116を標的としたCAR-T療法は、CBL変異クローンを選択的に攻撃できる可能性があり、CMMLに対する新たな治療選択肢として前臨床研究が進行中です。
③ がん免疫療法の新フロンティア:CBL-b特異的阻害剤
💡 用語解説:CBL-bとc-CBLの違い
c-CBLが主に骨髄系細胞のRTK制御を担うのに対し、CBL-bはT細胞・B細胞・NK細胞などの免疫細胞に高発現し、T細胞受容体(TCR)シグナルやサイトカイン産生を強力に抑制することで「免疫のブレーキ」として機能します。がん細胞は腫瘍微小環境においてこのCBL-bの抑制メカニズムを悪用し、T細胞の攻撃を逃れる「免疫回避」を引き起こしています。したがってCBL-bを薬理学的に阻害すれば、T細胞の抗腫瘍活性を持続・強化できると考えられています。
現在、製薬業界で最も注目を集めているのが、CBL-bを標的とした小分子阻害剤の開発です。代表的なパイプラインを紹介します。
特にNX-1607については、2025年のSITC(Society for Immunotherapy of Cancer)において、末梢血中の免疫活性化マーカー(pHS1陽性CD8 T細胞など)がベースラインから顕著に上昇し、腫瘍微小環境の免疫変調を引き起こす能力があることが臨床的に証明されました。CBL-b選択的阻害剤は、既存のPD-1/PD-L1阻害薬の限界を超える「次世代の免疫療法」として、がん治療の新たな柱となるポテンシャルを秘めています。
💡 用語解説:免疫チェックポイント阻害薬とは
PD-1・PD-L1・CTLA-4などの「免疫のブレーキ分子」をブロックすることで、がんに対する免疫攻撃を再活性化する薬剤です。一部のがんで劇的な効果を示しますが、すべての患者・がん種に有効ではないという限界があります。CBL-b阻害剤は免疫チェックポイント阻害薬とは異なる機序で作用するため、相補的な組み合わせによる相乗効果が期待されています。動物モデルでは単剤および抗PD-1抗体との併用で劇的な腫瘍増殖抑制効果と持続的な免疫記憶の形成が確認されています。
8. 遺伝カウンセリングの意義と実際
CBL遺伝子変異に関する遺伝カウンセリングは、特に以下の状況で重要になります。JMMLや骨髄系腫瘍と診断された患者ご本人・ご家族、またはCBL症候群(ヌーナン様症候群)との診断を受けた患者家族に対して、臨床遺伝専門医による遺伝カウンセリングが不可欠です。
- ➤JMMLと診断された全患者への生殖細胞系列検査の推奨:末梢血所見やDNAメチル化プロファイリングだけでは体細胞変異と生殖細胞系列変異を区別できないため、JMMLと診断された全例において生殖細胞系列の遺伝子検査を行うことが国際的に強く推奨されています。この結果が治療方針(Watch and Wait vs 早期移植)を直接左右します。
- ➤遺伝形式と家族への影響:CBL症候群は常染色体顕性遺伝ですが、多くはde novo(新生)変異です。患者本人が将来子どもを持つ場合の理論的遺伝確率は50%であり、この情報を含めたリプロダクティブプランニングについて丁寧に説明します。
- ➤出生前診断の選択肢:既知の変異が同定されている場合、絨毛検査・羊水検査による出生前遺伝子診断が選択肢として存在します。また、ミネルバクリニックが提供するNIPT Diamondプランでは、より包括的な出生前遺伝子情報を得ることも可能です。具体的な選択肢については専門医にご相談ください。
- ➤MRAによる血管炎スクリーニング:CBL変異を有するJMML患者に対しては、もやもや病や血管炎の合併リスクを念頭に置き、MRA(磁気共鳴血管画像)による定期的なスクリーニングが推奨されています。
- ➤心理的サポートと長期フォローアップ:CBL症候群の自然歴の蓄積は途上であり、希少疾患だからこそ長期的な医療機関との連携と継続的な情報収集が重要です。患者レジストリへの参加も選択肢の一つです。
9. よくある誤解
誤解①「CBL変異は白血病だけに関係する」
歴史的にJMML・CMMLなどの骨髄系腫瘍で発見されてきましたが、2024〜2025年の研究で小児CNS腫瘍・神経芽腫・胚細胞腫瘍などの固形腫瘍でも重要なドライバー変異であることが判明しています。CBL変異はRTK経路活性化の普遍的マーカーとして再評価されています。
誤解②「CBL変異のJMMLは全員移植が必要」
かつては全JMMLに対し速やかな骨髄移植が推奨されていましたが、現在は大きく変わっています。生殖細胞系列CBL変異によるJMMLの大部分は自然退縮を遂げることが多く、Watch and Watchが第一選択となっています。遺伝子検査の種類が治療選択の根拠となります。
誤解③「CBL-bとCBLは同じ遺伝子」
名前は似ていますが別の遺伝子です。c-CBLは主に骨髄系細胞でRTKシグナルを制御し、CBL-bは主にT細胞・NK細胞の免疫応答を抑制する「免疫のブレーキ」として機能します。がん免疫療法で開発が進むCBL-b阻害剤は、骨髄系腫瘍のCBL変異とは全く別の文脈で作用します。
誤解④「CBL症候群は遺伝するから親も同じ病気のはず」
CBL症候群の多くはde novo(新生)変異で生じており、両親には同じ変異が存在しないことがほとんどです。「両親が健康だから遺伝性疾患ではない」という誤解が診断を遅らせることがあります。常染色体顕性遺伝でもde novo変異による発症は珍しくありません。
よくある質問(FAQ)
🏥 CBL遺伝子変異・遺伝性腫瘍について専門医に相談する
JMMLのCBL変異、CBL症候群、遺伝子検査の選択に関するご相談は
臨床遺伝専門医が在籍するミネルバクリニックにお気軽にどうぞ。
関連記事
参考文献
- [1] Swaminathan G, et al. Molecular Pathways: Cbl Proteins in Tumorigenesis and Antitumor Immunity. Clin Cancer Res. 2015;21(8):1789-1794. [AACR Journals]
- [2] Sanada M, et al. Cbl and Human Myeloid Neoplasms: The Cbl Oncogene Comes of Age. Cancer Res. 2010;70(12):4789-4794. [AACR Journals]
- [3] Kobashigawa Y, et al. Autoinhibition and phosphorylation-induced activation mechanisms of human cancer and autoimmune disease-related E3 protein Cbl-b. PNAS. 2011;108(51). [PNAS]
- [4] Oncogenic Mechanisms of CBL E3 Ubiquitin Ligase Mutations in Myeloid Malignancies. Blood. 2019;134(Supplement_1):563. [ASH Publications]
- [5] Loh ML, et al. Molecular and phenotypic diversity of CBL-mutated juvenile myelomonocytic leukemia. Haematologica. 2021;106(8). [Haematologica]
- [6] Clinical and molecular features of CBL-mutated juvenile myelomonocytic leukemia. Haematologica. 2023. [Haematologica]
- [7] CBL mutations in chronic myelomonocytic leukemia often occur in the RING domain with multiple subclones per patient. PLoS One. 2024. [PLoS ONE]
- [8] Neven B, et al. First, Do No Transplant? Emerging Evidence for Watchful Waiting in Select JMML Patients. The Hematologist. 2026. [ASH Publications]
- [9] CBL mutations in pediatric solid and CNS tumors are a marker of receptor tyrosine kinase activation and a potential therapeutic target. bioRxiv. 2025. [bioRxiv]
- [10] Cbl-b inhibitor NX-1607 activates MAPK/ERK signaling pathway and enhances T-cell activation. PMC. 2025. [PMC]
- [11] Role of CBL Mutations in Cancer and Non-Malignant Phenotype. PMC. 2022. [PMC]
- [12] CBL Exon 8/9 Mutants Activate the FLT3 Pathway and Cluster in Core Binding Factor/11q Deletion AML/MDS Subtypes. Clin Cancer Res. 2009;15(7):2238-2247. [AACR Journals]
- [13] Discovery and Biological Evaluation of Novel, Potent, and Orally Available CBLB Inhibitors. J Med Chem. 2025. [ACS Publications]
- [14] CBL-related disorder. National Center for Advancing Translational Sciences (NCATS). [GARD/NIH]
- [15] Discovery and characterization of small molecule inhibitors of CBL-B that act as intramolecular glue. bioRxiv. 2026. [bioRxiv]